\n This email address is being protected from spambots. You need JavaScript enabled to view it.
), CBLU, University of Leeds
* revised and updated by: Marcus Hennecke, Ross Moore, Herb Swan
* with significant contributions from:
Jens Lippmann, Marek Rouchal, Martin Wilck and others -->
DOI: 10.1051/lait:2000142
Lait 80 (2000) 517-526
Plasmin digestion of bovine 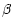 -casein dephosphorylated with one
protein phosphatase type 2A purified from Yarrowia lipolytica
-casein dephosphorylated with one
protein phosphatase type 2A purified from Yarrowia lipolytica
Pascale Joliveta - Isabel Queiroz Macedob - Min Wua
- Jean-Claude Meuniera
aLaboratoire de Chimie Biologique, INRA, INA PG, Centre de
Biotechnologies Agro-Industrielles, 78850 Thiverval-Grignon, France
bChemistry Department, University of Aveiro, 3810 Aveiro, Portugal
(Received 26 July 1999; accepted 16 May 2000)
Abstract:
Bovine
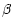
-casein was dephosphorylated by the catalytic sub-unit of a type 2A protein
phosphatase (PP2Ac) purified from the yeast
Yarrowia lipolytica. Complete
dephosphorylation was obtained after 24 to 30 h in Tris buffer (pH 7.5). On
the contrary, the activity of PP2Ac was largely inhibited (80%) in the presence
of 13 mmol
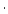
L
-1 sodium citrate (pH 6.8). After dephosphorylation of
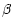
-casein,
plasminolysis was increased and more 3% TCA-soluble peptides were obtained
(30% increase). Dephosphorylation led to the disappearance of the f 29-105/107
peptide and to the appearance of a new non-phosphorylated 8 200 g
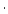
mol
-1 peptide,
suggested to be f 33-105/107 originated from the middle part of the
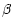
-casein
sequence and obtained upon plasmin cleavage of the Lys
32-Phe
33 peptide bond.
Keywords:
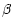 -casein / dephosphorylation / protein phosphatase / Yarrowia lipolytica / plasmin
-casein / dephosphorylation / protein phosphatase / Yarrowia lipolytica / plasmin
Résumé:
Hydrolyse par la plasmine de la caséine 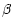 bovine déphosphorylée par une protéine
phosphatase de type 2A purifiée chez Yarrowia lipolytica.
bovine déphosphorylée par une protéine
phosphatase de type 2A purifiée chez Yarrowia lipolytica. La caséine
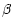
peut être
déphosphorylée par la sous-unité catalytique d'une protéine phosphatase de type 2A
purifiée chez la levure
Yarrowia lipolytica. La déphosphorylation complète est obtenue
en 24 à 30 h en tampon Tris (pH 7.5).
À l'inverse, elle est largement inhibée par le citrate
de sodium 13 mmol
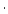
L
-1 à pH 6.8 (80 % d'inhibition). Après déphosphorylation, la
plasminolyse de la caséine
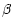
est augmentée puisque l'on observe une production
supplémentaire de 30 % de peptides solubles dans le TCA à 3 %. La déphosphorylation se
traduit par la disparition du peptide f 29-105/107 et l'apparition d'un nouveau peptide
non phosphorylé de 8 200 g
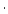
mol
-1. Il pourrait s'agir du peptide f 33-105/107 provenant
de la partie centrale de la séquence protéique de la caséine
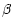
et obtenu par attaque de
la liaison peptidique Lys
32-Phe
33.
Mots clé :
caséine b / déphosphorylation / protéine phosphatase /
Yarrowia lipolytica / plasmine
Correspondence and reprints: Pascale Jolivet
tel. (33) 1 30 81 54 67; fax: (33) 1 30 81 53 73;
e-mail: This email address is being protected from spambots. You need JavaScript enabled to view it.
Copyright INRA, EDP Sciences
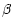 -casein dephosphorylated with one
protein phosphatase type 2A purified from Yarrowia lipolytica
-casein dephosphorylated with one
protein phosphatase type 2A purified from Yarrowia lipolytica![]() -casein / dephosphorylation / protein phosphatase / Yarrowia lipolytica / plasmin
-casein / dephosphorylation / protein phosphatase / Yarrowia lipolytica / plasmin


