\n This email address is being protected from spambots. You need JavaScript enabled to view it.
), CBLU, University of Leeds
* revised and updated by: Marcus Hennecke, Ross Moore, Herb Swan
* with significant contributions from:
Jens Lippmann, Marek Rouchal, Martin Wilck and others -->
DOI: 10.1051/lait:2000140
Lait 80 (2000) 491-501
Purification and characterization of an intracellular esterase
from Propionibacterium freudenreichii ssp. freudenreichii ITG 14
Evangellia Kakariari - Marina D. Georgalaki -
George Kalantzopoulos - Effie Tsakalidou
Laboratory of Dairy Research, Department of Food Science and Technology,
Agricultural University of Athens, Iera Odos 75, 118 55 Athens, Greece
(Received 17 December 1999; accepted 3 May 2000)
Abstract:
An intracellular esterase from
Propionibacterium freudenreichii ssp.
freudenreichii ITG 14
was purified by anion exchange and gel filtration chromatography. The enzyme
had a molecular weight of 47 400 g

mol
-1 as determined by gel filtration chromatography,
with an optimum activity on

-naphthyl-acetate at pH 6.0 and at 65
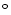
C,
with
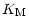
= 1.2 mmol

L
-1. The esterase hydrolyzed synthetic substrates of low molecular
weight (C2-C4), and among triglycerides only triacetin. Sulfhydryl group reagents and
metal chelators had limited or no effect on enzyme activity; highest inhibition was
observed with phenylmethyl sulfonyl fluoride (PMSF).
Keywords:
Propionibacterium freudenreichii ssp. freudenreichii / esterase /
purification / characterization
Résumé:
Purification et caractérisation d'une estérase intracellulaire de Propionibacterium
freudenreichii ssp. freudenreichii ITG 14. Une estérase intracellulaire extraite de
Propionibacterium freudenreichii ssp.
freudenreichii ITG 14 a été purifiée par
chromatographie échangeuse d'anions et chromatographie d'exclusion de taille.
L'enzyme avait une masse moléculaire de 47 400 g

mol
-1, comme déterminé par
chromatographie d'exclusion de taille, et elle avait une activité maximale sur le
substrat

-naphthyl-acétate à pH 6,0 et 65
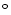
C, avec
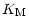
= 1,2 mmol

L
-1.
L'estérase dégradait des substrats synthétiques de faible poids moléculaire (C2-C4), et
parmi les triglycérides seulement la triacétine. Des groupements sulfydryles et des
chélateurs de métaux n'avaient aucun effet ou un effet limité sur l'activité
enzymatique ; la plus forte inhibition a été observée lors de l'utilisation du PMSF.
Mots clé :
Propionibacterium freudenreichii ssp. freudenreichii / estérase /
purification / caractérisation
Correspondence and reprints: Effie Tsakalidou
tel. (30) 1 529 4676; fax: (30) 1 529 4672;
e-mail: This email address is being protected from spambots. You need JavaScript enabled to view it.
Copyright INRA, EDP Sciences


